「この治療が効くかどうかは、やってみないとわからない」。これまでの医療では、そんな言葉が当たり前のように交わされてきた。だがいま、「効かないかもしれない」という不安を解きほぐす新たな医療のかたちが動き出している。それが、“その人に合った治療”を目指す「パーソナライズド医療(個別化医療)」だ。
遺伝子情報、体質、生活習慣、さらには免疫反応や心理的傾向まで、最新の科学は、患者一人ひとりの“医学的ポートレイト”を描くところまで進みつつある。パーソナライズド医療の現在地と未来について、がんと免疫の研究に取り組む立命館大学 薬学部の林嘉宏教授に聞いた。
● 「薬が効くか」は、もう“やってみないとわからない”ではない
● 遺伝子や免疫反応まで、“その人の医療”が見えてきた
● がん治療ではすでに個別化が進行、CAR-T療法も登場
● 睡眠・食事・体質──予防も“パーソナライズ”の時代へ
● 治療だけでなく、病気の“起こり方”に迫る
医療の“パーソナル化”で、より効果的な治療を受けられる時代へ
かつての医療は、「この病気にはこの薬、この治療法」という一律の考え方が主流だった。診断名に基づき、統計的に“多くの人に効果がある”治療法が選ばれる。それが医学の標準であり、合理的なアプローチとされてきた。
だが現実には、同じ診断を受けた患者であっても、治療の効果や副作用の出方には大きな違いがある。なぜ効く人と効かない人がいるのか――その問いに正面から向き合おうとする「パーソナライズド医療」について、がんと免疫を専門に研究する立命館大学・林嘉宏教授に解説いただこう。
「昔から、患者さんの状態に応じて治療を変えることは行われていました。ただ、それは主に症状や検査値など“目に見える範囲の情報”による判断でした。
しかし、最近になって、同じ病名でも、症状の原因や背景が『遺伝子レベルで違う』ということが見えるようになってきました。つまり、“同じ病気に見えても中身は違う”ということがわかるようになったのです」(林教授、以下同じ)
これまでの医療が“病気に対して人を当てはめる”ものだったとすれば、パーソナライズド医療は、“人に合わせて病気を理解し、治療法を考える”という方向への転換だという。
「今は、分子や遺伝子のレベルで個々人の病気の違いが見えてきて、新薬の開発にも生かされています。今後、よりパーソナルな治療が進んでいくのは間違いないでしょう。これは、10〜20年前には考えられなかったような進歩だと思います」
パーソナライズド医療の可能性が拓けてきた背景には、近年の医療・科学技術の急速な進歩がある。当事者である林教授自身も驚くほどの、現在の研究現場はどのようなものだろうか。
個人の遺伝情報の解析が「研究室で数時間」レベルで可能な時代
「昔は、“がん細胞を取って調べる”といっても、組織のかたまりとしての解析が限界でした。しかし今では、がんを構成する“1個1個の細胞”の違いまで見えるようになってきています。そして、パーソナライズド医療の実現を後押ししているのは、言うまでもなく、ここ10〜20年の間に起きた医学・生命科学領域における飛躍的な技術革新といっていいでしょう。
象徴的なのは、ゲノム解析技術の進歩です。かつて『ヒトゲノム計画』が始まったときは、世界中の研究者が10年以上かけて、ようやく1人分の全遺伝子配列を読み取るのが精一杯でした。ところが今では、それが“数時間”で終わる。しかも、1つの研究室でできてしまうレベルにまでコストも下がってきています。これは本当にとんでもない変化です」
こうした解析の簡易化と高速化によって、患者一人ひとりの遺伝的な違いや体の中で起きている反応を、分子レベルで「見える化」することが可能になった。だが、そこで得られるデータの量はあまりにも膨大だ。
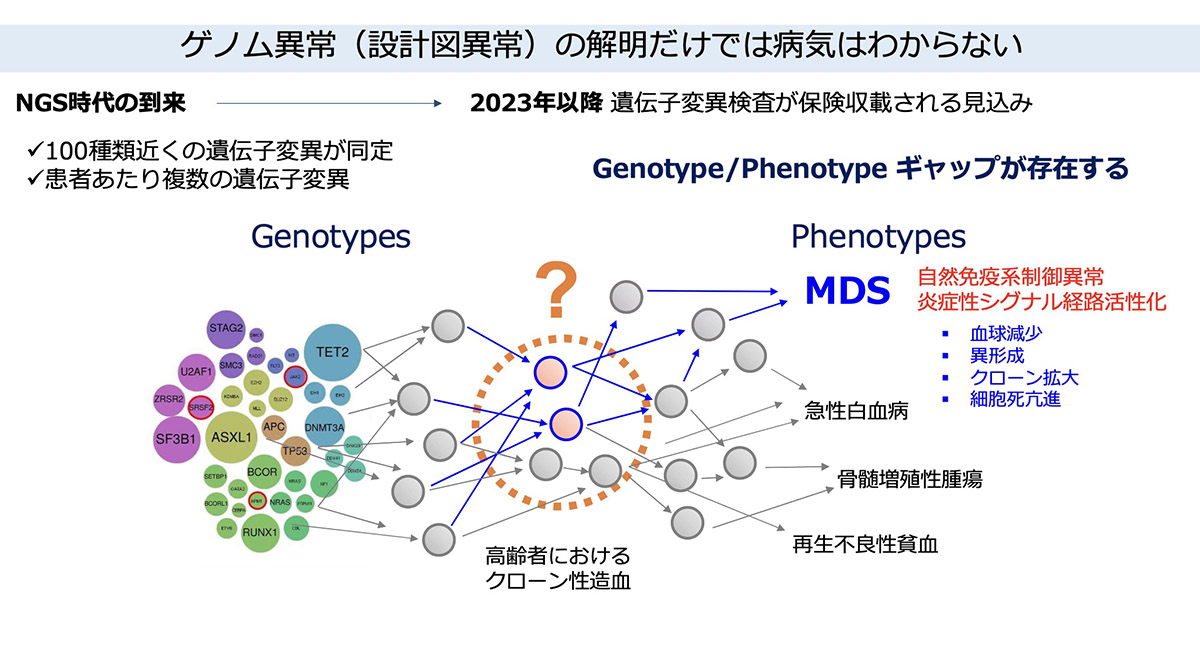
「実は、遺伝子の設計図だけではわからないこともたくさんあります。同じ遺伝子異常があっても、どう使われているか──たとえばメッセンジャーRNAがどう発現しているか、どんなタンパク質ができているか。それによって病気になるかならないかが変わる。そうした“出力”を見ないと、違いがわからないのです。
細胞ひとつひとつの違い、そこに関わる免疫細胞の動き、そして患者さんの体全体の環境……こうした複雑なデータを人間の頭だけで処理するのは、はっきり言って不可能です。そこで現在では、AIを活用して統合的に解析し、因果関係を導き出すというフェーズに入ってきています」
見えなかった“違い”が見えるようになり、それを読み解くための道具が揃ってきた。まさに今が、パーソナライズド医療の“地ならし”が終わりつつあるタイミングなのかもしれない。
がん治療で先行する“パーソナライズド医療”の実例
パーソナライズド医療が最も先進的に取り入れられている領域の一つが、がん治療だ。病名だけではなく、がん細胞の性質に応じて治療法を選ぶというアプローチは、すでに一部の疾患で実用化されている。
「たとえば乳がんでは、細胞の中にあるホルモン受容体やHER2というタンパク質の有無を調べて、それによって効く薬が変わってきます。こうした“分子の特徴”をもとにした治療は『分子標的治療』と呼ばれ、すでに当たり前のように行われています。
また、今では、特定のがんについて数十種類の遺伝子異常を一気に調べられる検査も、保険適用で可能になっています。その結果、“この異常があるならこの薬が効く”といった判断が、科学的に下せるようになってきました。まさにパーソナライズド医療の実現が現場で進みつつあるわけです」
そして、近年注目されているのが、患者自身の免疫細胞を用いたCAR-T(カーティー)細胞療法だ。
「CAR-T細胞療法では、患者さんから免疫細胞を採取して、体外で“がんにだけ反応するように改造”します。それを体に戻すことで、自分の免疫が自分のがんをやっつけてくれるようになる。これで劇的に効果が出る人もいます。まさに究極のパーソナライズド治療ですね」
現時点では、白血病や悪性リンパ腫といった血液がんの一部で実用化されているが、固形がんへの応用にはまだ課題が残るという。ただ、こうした“オーダーメイド型の免疫治療”が広がっていけば、抗がん剤に頼らない新たな治療の道が拓ける可能性もある。
一方、先進的な治療には現実的な課題もある。現在のCAR-T細胞療法の費用は1回あたり約3,000万円とされ、経済的なハードルは極めて高い。
「最初は高額でも、普及と技術の進化によっていずれはコストが下がり、より多くの人が恩恵を受けられるようになるはず」と林教授は語る。高度なパーソナライズド治療が、誰にとっても“手が届くもの”になる未来は、患者にとって大きな希望となる。
生活習慣病などにも“パーソナライズド医療”が広がる
パーソナライズド医療は、がんのような重篤な病だけに限られた医療ではない。生活習慣病や慢性疾患といった“身近な病気”の領域にも、その考え方が広がり始めている。
「たとえば生活習慣病。これまで『食べすぎ』『運動不足』といった一律の原因で語られがちでしたが、実際には患者さんごとに体の中の反応が異なることがわかっています。同じような生活をしていても、炎症が起きやすい人もいれば、そうでない人もいる。近年の研究で、その違いが遺伝子の“使われ方”にあることもわかってきました。
設計図(遺伝子)に異常がなくても、実際にどんなタンパク質が作られているか、どの免疫細胞が活性化されているか。そのバランスが崩れることで病気が起きているケースも多いのです」
こうした“見えにくかった体内の違い”は、今ではさまざまな実験や研究によって徐々に明らかになりつつある。たとえば睡眠不足が慢性的な炎症を引き起こし、動脈硬化を進行させることや、特定の食事が免疫反応に影響を与えることも、科学的に裏付けられてきた。
「同じ生活習慣でも、誰にどんな影響が出るかは人によって違う。その違いが分かれば、“この人にはこういう生活改善が有効”と、より精度の高い予防ができるようになるはずです。予防医療も含めて、パーソナライズドにできる余地はまだまだあります。がん以外の病気でも、個人に合わせたアプローチが確実に必要になってきています」
病気になってから考える時代から、自分の身体を理解して、先回りして選ぶ時代へ。パーソナライズド医療は、未来の健康観そのものを変えようとしている。
病気の周囲を含めて、“その人に起きていることを理解する”
がん治療の最前線では、細胞の中を覗き込み、遺伝子やタンパク質の振る舞いを観察する時代が始まっている。しかし、林教授の視線は“それだけ”にはとどまらない。
「がん細胞だけを見ていても、治療の限界がある──それがここ数年の私の実感です。実は、がんの周囲にいる免疫細胞や他の細胞たちが、がんの進行や患者さんの体調に深く関わっていることがわかってきたのです」
林教授の研究では、がん細胞を単体で扱うのではなく、“がんという現象が起こっている体全体”を一つの環境として捉える。その中で、がんの成長や治療抵抗性、そして全身症状の原因を探っている。
「たとえば、がん患者さんが痩せていく現象があります。実はその背後に、これまで知られていなかった免疫細胞の働きがあることがわかってきました。がんが進行すると、体内で特殊な免疫細胞が現れて、筋肉を分解するような反応を引き起こすのです」

これまで「副作用」や「体力低下」と片づけられてきた現象が、実はがんと免疫系との精緻なやりとりによって引き起こされていたのだ。そうした“体の声”に耳を澄ませる研究が、いま進んでいる。
「私たちのチームでは、がん細胞そのものに注目するだけでなく、その周囲で何が起きているのか──つまり患者さんの体の中全体で、病気という現象がどのように進行しているのかを包括的に捉えようとしています。細胞の種類ごとに遺伝子の働きを調べ、タンパク質の動態を解析し、ときには免疫系や筋肉組織の変化まで追いかける。そうして初めて、“なぜこの患者で病気が悪化するのか”“なぜこの治療が効かないのか”といった問いに、本当の意味で近づけると思います。
病名ではなく、“その人に起きていること”を理解する。私はそこに、これからの医療の本質があると思っています」
この視点が導くのは、“治療”にとどまらない未来だ。がんがどう起こり、どう広がり、どう止められるかを理解できれば、「治す」だけでなく「防ぐ」ことにもつながる。林教授の研究は、新たなパーソナライズド医療の突破口を拓こうとしている。

林 嘉宏
滋賀で生まれ育つ。2005年に滋賀医科大学医学部医学科を卒業し、血液内科医として勤務。2013年に滋賀医科大学大学院博士課程を修了。米国シンシナティ小児病院医療センター実験血液学・腫瘍生物学部門での勤務(2013年~2017年、博士研究員)を経て、2017年より東京薬科大学生命科学部 講師(2020年より准教授)。2023年に立命館大学薬学部に着任し、現在に至る。臨床での課題を起点として、病気がおこるしくみの解明と新規治療法の開発に取り組んでいる。