アスリート、特に持久系種目においては「房室ブロック」と呼ばれる不整脈の発生頻度が高いことが知られている。房室ブロックは心拍を促す電気信号に異常があることがわかっていたが、そのメカニズムの全容はわかっていない。しかし今回、心臓ペースメーカ組織に関連する、新たな分子メカニズムが解明された。
● 心臓の鼓動と「心臓ペースメーカ組織」の関係
● 軽度では成人の10%が該当する「房室ブロック」
● 一般的な運動は問題なし! むしろ運動の効果を優先すべし
● イオンチャネルの機能低下を引き起こすマイクロRNA
● 機械式ペースメーカを超える新たな治療法開発に期待
鼓動は「心臓ペースメーカ組織」の電気信号から生まれる
心臓の筋肉は微弱な電気信号を受け取ることで収縮し、全身へ血液を送り出すポンプ運動を営む。この心拍動を生み出す電気信号を作り出し、伝導させる組織が、「心臓ペースメーカ組織」と呼ばれる部分だ。
しかし、その心臓ペースメーカ組織が正常に働かなくなると、安静にしている時の心拍数が異常に低くなり、いわゆる不整脈の状態になることがある。

立命館大学 生命科学部 生命医科学科講師の中尾周氏は、その不整脈の1つである「房室ブロック」について、心臓ペースメーカ組織の機能に関連する「心臓イオンチャネルたんぱく質」の機能障害を突き止め、さらにたんぱく質をコードしない遺伝子DNA領域から生成されるマイクロRNAが関与していることを解明した。
成人の10人に1人? アスリートに多い「房室ブロック」とは
「房室ブロックとは、不整脈の一種で、心房から心室へ送る電気信号の伝達が不完全、あるいは遮断された状態のことです。心臓は、心房と心室が適切なタイミングで交互に収縮することで効率的に血液を送り出しますが、房室ブロックでは、心房と心室の連動が悪くなり、心臓の血液を送り出す効率が低下するのです」(中尾講師、以下同じ)
また、同じ房室ブロックでも、ほとんど無症状の第1度から、機械式ペースメーカを植込まなければならない第3度まで、重症度によって段階がある。
「第1度の場合は、状態が悪くなることはほとんどありません。まれに第2度に進行することもありますが、確率は低いとされています。第2度はいい状態と悪い状態を行ったり来たりする段階。第2度の重症例や第3度の場合は、悪い状態がずっと続くため、機械式ペースメーカを植込まなければならなくなります。
この“悪い状態”とは、心臓が血液を送り出す回数が減っている状態です。通常心拍は毎分60〜100回ほどですが、房室ブロックが起こると、1分間に20回程度まで減少します。人間は6〜10秒心臓が止まればめまいを起こし、心臓が止まってしまうこともあるので、3秒に1回しか心拍がないのは、ふらつきを起こすほどの状態といえます」
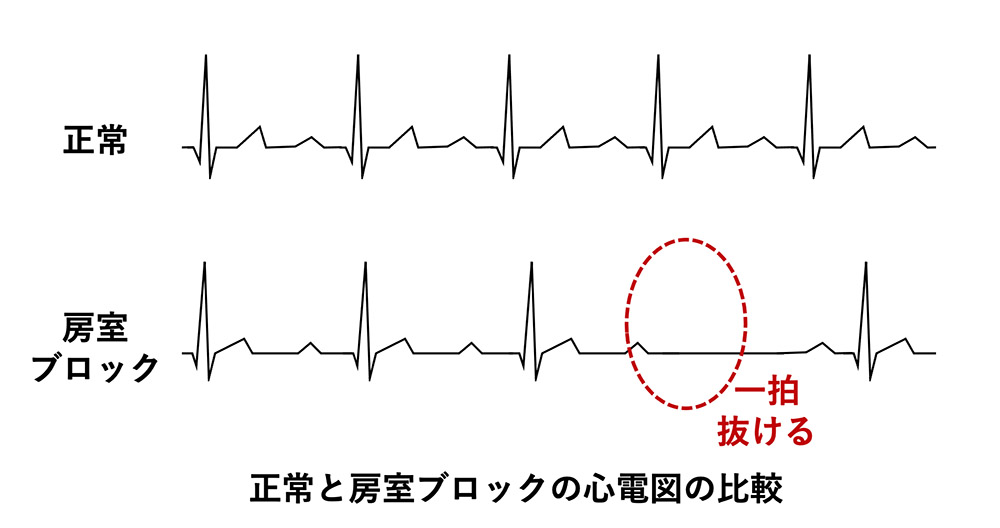
症状の軽い第1度を含めると、成人のおよそ10人に1人の確率で房室ブロックは起こるという。特に持久系スポーツのアスリートに多いとされているが、現在のところ、特定の競技との因果関係は明らかになっていない。
ここで注意したいのは、房室ブロックはあくまでアスリートレベルでのトレーニングを長期間行った場合の話であるという点だ。適度な有酸素運動や、一般人が趣味や健康のために行う程度の運動であれば、心血管病の予防や、メタボリックシンドロームの予防など、メリットの方が大きい。くれぐれも、房室ブロックを恐れて運動を控えることがないようにご注意を。
「電気信号の通り道」となるたんぱく質の生成を阻害するRNAを特定
詳細なメカニズムが不明で、自律神経など心臓の外からの作用が関連しているとも考えられてきた房室ブロックだが、中尾氏らの研究により、根本原因のひとつである心臓の分子メカニズムが明らかになった。
「今回の研究では、持久運動によって心臓ペースメーカ組織の機能が低下したマウスおよびウマで、房室結節でイオンチャネルたんぱく質の量と機能が低下していることが判明しました」
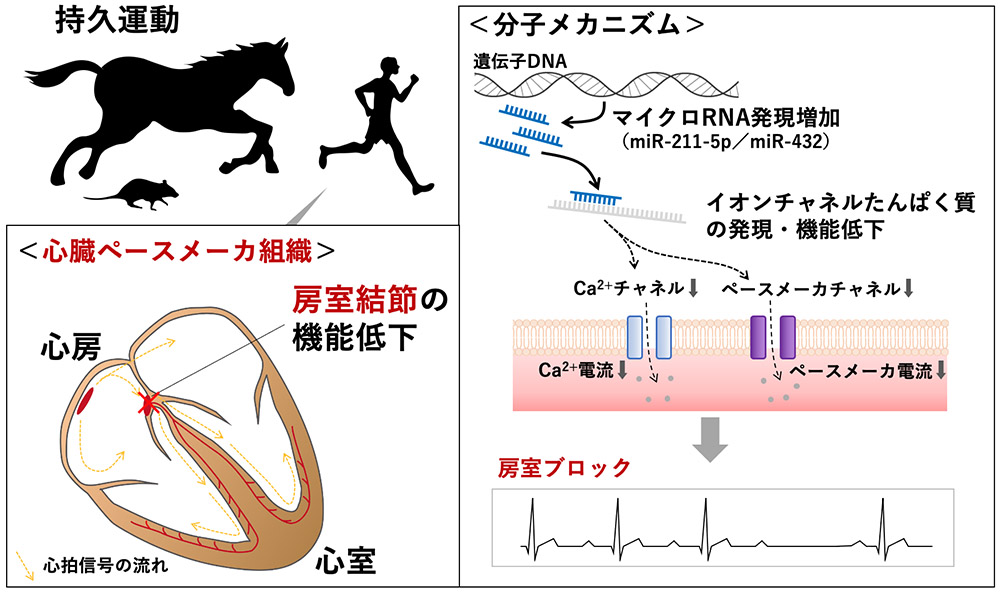
イオンチャネルたんぱく質とは、心臓の細胞膜上にある膜タンパク質のことで、それぞれ特定のイオンを出し入れすることにより電気信号を生み出している。ペースメーカチャネルをイオンが通過することで鼓動を促す信号のきっかけを作り、さらにカルシウムチャネルやカリウムチャネルなど複数のイオンチャネルが協調して、その信号を心臓全体へ伝えることで心室筋が収縮する、という具合だ。
ではなぜ、イオンチャネルたんぱく質の機能低下が起きるのだろうか。
「遺伝子DNAの中には、イオンチャネルたんぱく質を生成するための情報が組み込まれています。しかし、その生成途中のたんぱく質を壊すマイクロRNAという阻害物質が、遺伝子DNAの別の領域から作られています。
1つのマイクロRNAが標的にしている遺伝子は非常に多く、働きの因果関係を特定するのは非常に困難です。そんな中で、少なくとも2つのマイクロRNA(miR-211-5p、miR-432)が、イオンチャネルたんぱく質の発現を抑制することを特定したという意味で、大きな成果といえます」
この成果は、「マクロからミクロまで」にわたって詳細に心臓を分析してきた成果だと、中尾氏は語る。心臓の解析、心臓から取り出した細胞の解析、たんぱく質や遺伝子の解析など、多くの共同研究者による地道な取り組みが、新発見につながっている。
ペースメーカ手術のリスクを減らし、不整脈患者に新たな治療の選択肢を

現在、重度の不整脈患者の治療には、機械式ペースメーカの植込みしか選択肢がない。しかし、徐々に不整脈メカニズムの解明が進むことで、よりよい予防・治療法が確立される可能性が高まっていく。
「今回はマイクロRNAが不整脈の原因であり、治療対象となり得るという点で、新たな治療法に結びつく成果だったと考えています。ただ、運動によってさまざまな変化が全身や心臓に起こりますが、そのどれが房室結節に直接影響を与えたのかはわかっていません。今後は、心臓内の電気伝導に影響を与える刺激を特定し、新たな治療標的を見出すための研究を続けていきます。
今後、マイクロRNAを心臓ペースメーカ組織で抑制する方法が確立されれば、不整脈の予防にもつながると考えています。アスリートに発生する房室ブロックや徐脈などの不整脈は、現役時代に支障がなくても、中高齢になってから治療が必要になるリスクもはらんでいるので、現役時代から何らかの手立てができれば症状を抑えることもできるはずです」
また、マイクロRNAには多くの種類があり、房室ブロックだけでなく、がんや免疫疾患、筋肉疾患にも関与しているという。今後、マイクロRNAを病気の臓器だけで抑制する方法が開発されれば、不整脈に悩むアスリートだけでなく、その他多くの患者の希望となるはずだ。
さらに中尾氏の目指す未来には、新たなペースメーカ治療のイメージもある。
「私たちのもう1つの最終目標は、心臓ペースメーカ細胞を人工的に作り出す方法の研究です。心臓ペースメーカ組織の特徴を突き詰め、患者由来の細胞や心臓にペースメーカ機能を持たせる再生療法を確立していきたいと考えています」
自らの細胞由来の心臓ペースメーカ細胞ができれば、機械式ペースメーカと比較して、極めて低侵襲かつ安全性の高い不整脈治療が可能になる。道のりはまだ長いが、中尾氏らの地道な基礎研究によって、確実にその未来への距離は縮まっている。

中尾周
岐阜大学大学院連合獣医学研究科修了、博士(獣医学)。国立循環器病研究センターおよび英国マンチェスター大学心血管科学研究所 ポスドク、立命館大学生命科学部生命医科学科 助教を経て、現在は同学科 講師として応用分子生理学研究室 主任研究者を務める。専門は心臓生理学、再生医学、分子生物学。趣味はマラソン、山歩き。